Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Memorias del Instituto de Investigaciones en Ciencias de la Salud
On-line version ISSN 1812-9528
Mem. Inst. Investig. Cienc. Salud vol.5 no.2 Asunción Dec. 2007
COMUNICACIÓN CORTA
Precisión y exactitud de un método enzimático para la determinación de colesterol total
Precision and accuracy of an enzimatic method for total cholesterol determination
*Rodríguez N, Velásquez Y, González E, Lorente A
Grupo de Investigación en Aseguramiento de la Calidad y Análisis Clínicos
Escuela de Bioanálisis. Facultad de Farmacia y Bioanálisis. Universidad de Los Andes Campo de Oro. Mérida-Venezuela
RESUMEN
El acoplamiento de las enzimas colesterol esterasa, colesterol oxidasa y peroxidasa es uno de los métodos mas empleados para la determinación de colesterol. La formulación de Allain y col. y la modificación de Roeschlau ha sido adaptada por Laboratorios Heiga en su reactivo Ref 450-L para la determinación en suero; planteando la necesidad de determinar su confiabilidad. Así, el objetivo de este trabajo es evaluar la exactitud y precisión del mismo. Para ello, se efectuaron 30 determinaciones consecutivas del analito en ensayos controles de dos niveles de concentración (CN: 193 mg/dL y CA: 247 mg/dL) y 30 ensayos de adición (R: agregando 200 mg de colesterol al CN). La precisión intralaboratorio se determinó mediante los coeficientes de variación (CV) y la precisión interlaboratorio con la Desviación Estándar Obtenida (DEO). La exactitud se evaluó con el porcentaje de recuperación (%R) y el Desvío Relativo Porcentual (DRP) de la media obtenida con respecto al valor del CN (determinado por un Laboratorio de Referencia). Los CV oscilaron entre 0,63% y 1,13% y las DEO entre -1,70 y -0,18; considerándose ambos satisfactorias (CV menores a 5% DEO entre – 2 y + 2). El %R fue de 104,8% y el DRP del CN de 0,89%, considerándose aceptables por encontrarse entre 95 y 105% y menor a 9%, respectivamente. Se concluye que el método evaluado presenta precisión intralaboratorio e interlaboratorio así como exactitud para niveles normales y altos de colesterol.
Palabras claves: Precisión, exactitud, confiabilidad.
ABSTRACT
The coupling of enzymes cholesterol esterase, cholesterol oxydase and peroxydase is the most frequently used method to determine cholesterol. The Allain et al formulation and Roeschlau et al modification have been adapted by Heiga Laboratories in its Ref 450-L reagent to determine total cholesterol in serum; establishing the necessity of evaluating its reliability. Thus, the objective of this research is to evaluate the accuracy and precision of this method. For this, 30 consecutives determinations were carried out in control assays at two concentrations levels (NC: 193 mg/dL and AC: 247 mg/dL) and 30 addition assays (R: adding 200mg of cholesterol to NC). The intra-laboratory precision was determined using variation coefficients (VC) and the inter-laboratory precision with the Obtained Standard Deviation (OSD). The accuracy was evaluated with the recovery percentage (%R) and the percent relative deviation (PRD) of the mean obtained in relation to the NC value(established by a Reference Laboratory). The VC ranged from 0. 63% to 1.13% and the OSD between -1.70 and -0.18 and they were both considered satisfactory (VC lower than 5% and OSD between -2 and +2). The %R was 104.8% and the PRD was 0.89%, being considered acceptable because the values were between 95% and 105%, and lower than 9% respectively. It was concluded that the evaluated method shows intra-laboratory and inter-laboratory precision as well as accuracy for normal and high cholesterol levels.
Keywords: Precision, accuracy, reliability.
INTRODUCCIÓN
El acoplamiento de las enzimas colesterol esterasa, colesterol oxidasa y peroxidasa ha sido propuesto como posible método de referencia (1) y es uno de los métodos mas empleados para la determinación manual de colesterol (1,2). El mismo ha sido adaptado por Laboratorios Heiga de la formulación de Allain y col. (3) y la modificación de Roeschlau y col. (4) en su reactivo Ref 450-L (5), planteando la necesidad de determinar su confiabilidad.
La confiabilidad de un método analítico es su capacidad para realizar análisis proporcionando resultados adecuados, la misma incluye diversos parámetros como exactitud, precisión, sensibilidad, especificidad, linealidad y paralelismo (6,7).
La exactitud refleja la concordancia aproximada entre el valor obtenido en una medición y la cantidad real existente en el material examinado. Este parámetro es considerado como el más importante de todos ya que su correspondencia con el valor real de la medición no puede existir sin la positividad de los demás parámetros mencionados. Para su determinación se disponen de cuatro procedimientos: prueba de la adición o recuperación, prueba de la mezcla, prueba de comparación y la utilización de la fórmula de Murali Dharán modificada en su aplicación por González y Lorente (Desviación Estándar Obtenida= DEO) (8), si se dispone del valor real (o de referencia) del material de control empleado(9).
Por su parte, la precisión expresa la concordancia de una serie de determinaciones entre si con respecto a su media. Para determinarla se utilizan tres parámetros estadísticos que son: la desviación estándar (DE), la varianza y el coeficiente de variación (CV)(10). También puede emplearse la Desviación Estándar Obtenida, pues esta refleja la dispersión del resultado con respecto al valor aportado por el fabricante del material de control o del laboratorio de referencia(9).
Se conoce que los métodos enzimáticos para la determinación de colesterol en suero han presentado buenos resultados al probar su confiabilidad (1), por lo cual es posible que el método de la casa comercial HEIGA presente igual comportamiento; siendo el objetivo de este trabajo el de evaluar la precisión intralaboratorio e interlaboratorio y la exactitud del referido método.
MATERIALES Y MÉTODOS
Se llevaron a cabo 30 determinaciones consecutivas de colesterol en sueros controles de dos niveles de concentración: dentro (CN) y superior (CA) al rango de referencia del analito (CN: 193 mg/dL y CA: 247 mg/dL). Estos sueros correspondían al CN que es un suero control humano liofilizado valorado por el Laboratorio de Referencia y Estandarización (LARESBIC) de la Fundación Bioquímica Argentina, lote 348 y el CA a un suero control Hematronix (Hematronix, INC. 524 Stone Benicia, CA 94510) liofilizado, lote 229.
Con los resultados obtenidos se calculó la media (VO) y desviación estándar (DE) y con estos datos se determinó la precisión intralaboratorio a través del coeficientes de variación [CV = (DE / VO) x 100]. Mientras que la precisión interlaboratorio se evaluó por la fórmula para Desviación Estándar Obtenida (DEO) de Murali Dharán (11) (modificada en su aplicación por González y Lorente (DEO = VE – VO/DEE) (12), en la cual el VE correspondía al valor del suero control y DEE a un 5% de este valor, considerándose que ésta era satisfactoria si aportaba valores entre -2 y +2.
Para la evaluación de la exactitud se determinó el Desvío Relativo Porcentual (DRP) de recuperación (%R). El DRP consiste en la expresión porcentual del desvío del valor obtenido con respecto al valor real y se determinó con la expresión: DRP= [(VE-VO/VE)x 100] (13, 14). Por su parte, el porcentaje de recuperación se obtuvo con los resultados de 30 determinaciones consecutivas de colesterol en ensayos de recuperación preparados con e agregado de 200 mg del analito (mediante un patrón de 200 mg/dl) al CN (15).
Se consideró exactitud positiva si el DRP era menor o igual a 9% (13, 14) y el %R se encontraba entre 95 y 105% (15).
El estudio se efectuó en el Laboratorio de Bioquímica Clínica de la Escuela de Bioanálisis de la Universidad de Los Andes (Mérida-Venezuela), efectuando las mediciones de absorbancias en un espectrofotómetro Stasar IV marca Gilford (Ohio, USA) y la calibración con un estándar de 200 mg/dL, provisto por el fabricante del reactivo.
RESULTADOS
En la tabla 1 se muestran los resultados del estudio de precisión; en la misma puede apreciarse que la precisión intralaboratorio fue satisfactoria al presentarse CV inferiores a 5%. Por su parte, la precisión interlaboratorio, reflejada en términos de las DEO resultó también adecuada al presentar valores inferiores a ±2 (12).
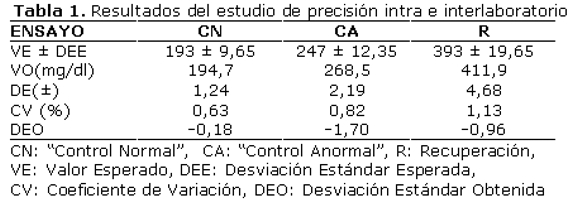
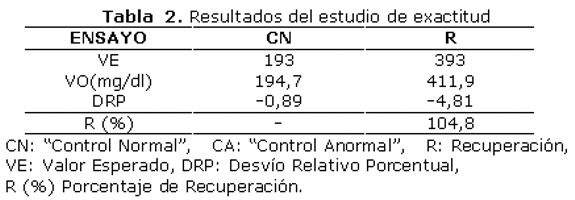
En relación a la exactitud (tabla 2), la prueba de adición arrojó un %R satisfactorio al encontrarse en el rango de 95 a 105% y los DRP para el CN y el ensayo de R también indicaron la presencia de exactitud, por resultar inferiores a 9%.
Al analizar los DEO de todas las determinaciones (figura 1), destaca el hecho de que, salvo una determinación en el CN, las DEO en los ensayos CN y CA fueron inferiores a 0.
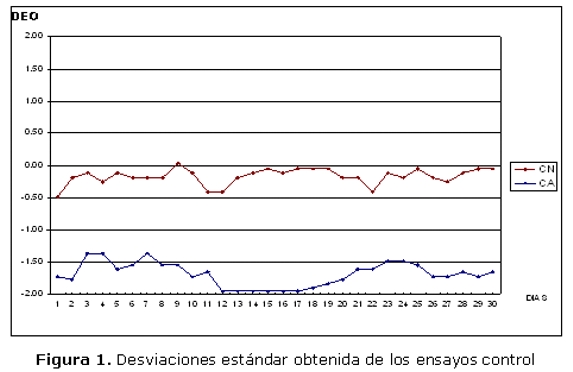
Se presentan los resultados diarios de Desviación estándar obtenida (DEO) para los ensayos CN (Control Normal) y CA (Control Anormal); puede observarse que casi el 100% de los datos son negativos, presentándose el CN entre 0 y -0,5 y CA entre el valor -1 y -2.
DISCUSION
Los CV inferiores a 5% obtenidos en el estudio de precisión intralaboratorio indican el cumplimiento de este requisito para las metodologías cortas y la posibilidad de obtener resultados con poca dispersión y reproducibles con su utilización (14).
Los valores negativos de DEO, casi en un 100%, indican que los resultados fueron superiores al valor esperado, posiblemente por un error sistemático positivo en la calibración (14), ya que el hecho se repite en los dos materiales de control empleados. Además, esto correlaciona con el %R superior al 100%, indicando que las determinaciones que se efectúen con el mismo pueden resultar ligeramente superiores al valor real; sin embargo, tal error se considera aceptable al no exceder el límite del error máximo tolerable al considerar tanto el error sistemático como el aleatorio encontrados(6).
De acuerdo a los resultados obtenidos se concluye que el método evaluado presenta buena precisión intralaboratorio e interlaboratorio así como exactitud para niveles normales y altos de colesterol.
Es recomendable evaluar otros parámetros de confiabilidad del método como linealidad, sensibilidad y especificidad en los niveles de este estudio.
BIBLIOGRAFIA
1. Naito H. Colesterol. En Kaplan, L, Pesce A. Triglicéridos. Química Clínica. (2da edición). Editorial Médica Panamericana. Buenos Aires. 1.990: 1164-86. [ Links ]
2. Salve M, Amich S, Prieto S, Casas A. Bioquímica, laboratorio clínico. Editorial Interamericana Mc Graw-Hill. Madrid. 1994: 61-2. [ Links ]
3. Allain C, Poon, L, Chang, C Richmond W, Fu P. Enzymatic determination of total serum cholesterol. Clin Chem 1974; 20: 470-475. Comentado en: Laboratorios Heiga, C.A. Reactivos para Laboratorios Clínicos. Determinación in Vitro del colesterol total. Enzimático líquido. Ref. 450-L. 2004. [ Links ]
4. Roeschlau P, Bernt E, Gruber W. Enzymatic determination of total cholesterol in serum. A Z Klin Chem Klin Biochem 1974; 12(5):226. Comentado en: Laboratorios Heiga, C.A. Reactivos para Laboratorios Clínicos. Determinación in Vitro del colesterol total. Enzimático líquido. Ref. 450-L. 2004. [ Links ]
5. Laboratorios Heiga, C.A. Reactivos para Laboratorios Clínicos. Determinación in vitro del colesterol total. Enzimático líquido. Ref. 450-L. 2004.
6. Boquet E, Castillo M, Cáceres A, Dybkaer R, Escutia V, Francini C, et al. Mejoría continua de la calidad. Guía para los laboratorios clínicos de América Latina. Confederación Latinoamericana de Bioquímica Clínica. Editorial Médica Panamericana. México. 1996: 53-68, 239-45. [ Links ]
7. Rodríguez N, Lorente, A, Velásquez Y, González E. Confiabilidad del método Slott modificado por Laboratorios Heiga para la determinación directa de la Creatinina. Revista de la Facultad de Farmacia. 2001; 42:67-8. [ Links ]
8. Rodríguez N, Torres D, Carvajal M. Confiabilidad del método de Jaffé modificado por Laboratorios Heiga para la determinación automatizada de la Creatinina. Revista de la Facultad de Farmacia. 2001; 42:55-7. [ Links ]
9. Mujica X, Santiago G, Vivas S. Precisión y exactitud del método enzimático de Heiga para le determinación de triglicéridos (Trabajo de Grado) Mérida (Venezuela): Universidad de Los Andes, 2004. [ Links ]
10. Rodríguez N, Labrador Z, González E, Lorente A. Método Slott modificado por Heiga para la valoración de Creatinina: confiabilidad a 25ºC en el IMPACT 400E. Revista de la Facultad de Farmacia. 2002; 44: 59-60. [ Links ]
11. Dharan M. Control de calidad de los técnicos en: Control de calidad en los laboratorios clínicos. Editorial Reverté. España, 1982: 181-92. [ Links ]
12. González S, Lorente A. Sistema Básico de Control de Calidad. Universidad de Los Andes. Mérida-Venezuela. 1.994: 12-3. [ Links ]
13. Fundación Bioquímica Argentina. Programa de Evaluación Externa de la Calidad. Criterios de Aceptabilidad. 2005. [ Links ]
14. Fernandez C, Mazziotta D, directores. Gestión de Calidad en el Laboratorio Clínico. Confederación Latinoamericana de Bioquímica. Editorial Médica Panamericana. 1º Edición. Buenos Aires, 2 005: 401. [ Links ]
15. Gella J. Metrología en el laboratorio Clínico. BioSystems, S. A. 1.998: 8-35. [ Links ]
*Autor Correspondiente: Dra. Norys Rodríguez
Teléfono: 58-274-2715927
E-mail: norysr@ula.ve, giacac@ula.ve*














