INTRODUCCIÓN
Hasta el brote de SARS en 2002, durante el cual los coronavirus (CoV) demostraron su potencial de propagación epidémica y su patogenicidad significativa en los seres humanos, se los conocía principalmente como causas de enfermedades respiratorias y gastrointestinales leves1. La enfermedad por coronavirus 2019 (COVID-19) es causada por el virus SARS-CoV-2, que es un patógeno emergente identificado inicialmente en Wuhan, China, en diciembre de 20192.
Al momento de la presentación de esta revisión el SARS-CoV-2 ha infectado a más de 2,6 millones de personas en todo el mundo y se cobraron 185.000 vidas, amenazando a muchas más3. Esto conlleva una letalidad del 2,5% con una extensión mayor que las anteriores epidemias por SARS-CoV y MERS4.
Se estima que alrededor de 14% de los pacientes con COVID-19 desarrollan síntomas respiratorios que requieren oxígeno suplementario, y aproximadamente el 5% desarrolla una necesidad de ventilación mecánica5. Los CDC informan una tasa general de letalidad de 2,3%, aunque es más alta (14,8%) en pacientes mayores de 80 años y 49% en enfermos críticos requiriendo ventilación mecánica6.
El 16 de junio de 2020 se publicó el informe preliminar del estudio RECOVERY que comparó a los pacientes con neumonía COVID-19 que recibieron dexametasona 6 mg por día durante un máximo de 10 días (o hasta el alta hospitalaria) contra aquellos que no recibieron corticosteroides. En este estudio, la mortalidad fue menor en los pacientes que recibieron dexametasona en comparación con el grupo que no la recibió. Aunque la disminución de la mortalidad fue de 11% en pacientes con ventilación mecánica invasiva (29% vs. 40%), la diferencia en la mortalidad global fue muy estrecha (22,9% vs. 25,7%)7.
Teniendo en cuenta los resultados del estudio RECOVERY, la mayoría de las guías de gestión hospitalaria a nivel mundial la incluyeron. Sin embargo, hasta ahora no está claro si el tratamiento para las complicaciones del COVID-19, síndrome de dificultad respiratoria aguda (SDRA) o síndrome de liberación de citoquinas, es un efecto particular de la dexametasona o es un efecto que también puede obtenerse con otros corticosteroides, incluso si las dosis bajas o altas de los mismos son similares en este efecto8.
El objetivo de este estudio fue comparar la mortalidad de los pacientes internados medicados con dexametasona en comparación con metilprednisolona en el tratamiento de la neumonía por SARS-CoV-2 en el bloque modular respiratorio del Hospital Nacional, Itauguá, Paraguay, en el periodo de mayo a julio de 2021.
METODOLOGÍA
Se aplicó un diseño ambispectivo. Se incluyeron a pacientes internados con neumonía por SARS-CoV-2 confirmada por hisopado nasofaríngeo mediante la reacción en cadena de la polimerasa de transcripción inversa en tiempo real que cumplían con el protocolo de Berlín, con saturación por oxímetro de pulso menor a 92% con aire ambiente y confirmación imagenológica por radiografía o tomografía axial computarizada de tórax.
El muestreo fue no probabilístico por conveniencia. No se calculó el tamaño de la muestra porque se incluyeron a todos los pacientes que recibieron 6 mg de dexametasona o 200 mg de metilprednisolona que estuvieron internados en el bloque modular 11 del Hospital Nacional de Itauguá.
Luego de haber firmado el consentimiento informado, los pacientes que requirieron oxigenoterapia suplementaria fueron tratados según el protocolo institucional dentro del periodo comprendido entre el 1 de mayo y 31 de junio de 2021 con dexametasona 6 mg/día endovenoso al día por un máximo de 10 días o hasta el alta hospitalaria. A partir del 1 de julio de 2021 hubo una provisión irregular de la dexametasona en los hospitales públicos por lo que se optó por utilizar metilprednisolona en dosis de 1,5 mg/kp/día. Esta dosis se basó en reportes del manejo del SARS-CoV-2 y las neumonías fulminantes y organizativas. En todos los casos se logró la suspensión brusca de corticoides debido a que no sobrepasaron los 10 días con dicha medicación. Todos los pacientes recibieron 12 mg/día de ivermectina por 2 días consecutivos como prevención contra el síndrome de Loeffler. Estos grupos fueron pareados teniendo en cuenta la morbilidad. Los participantes fueron seleccionados por una tercera persona ajena al grupo de investigación en 2 grupos de análisis:
Grupo 1: pacientes con neumonía por SARS-CoV-2 que recibieron 6 mg de dexametasona endovenosa por diez días o hasta el alta.
Grupo 2: pacientes con neumonía por SARS-CoV-2 que recibieron metilprednisolona 1,5 mg/kp/día por 10 días o hasta el alta.
Se excluyeron pacientes con infección asintomática por SARS-CoV-2, pacientes con contraindicación conocida a los corticoides y pacientes fallecidos por otras causas (procesos expansivos cerebrales, accidentes cerebrovasculares masivos).
Todos los pacientes recibieron tromboprofilaxis con heparina de bajo peso molecular y fueron sometidos a estudios laboratoriales (hemograma, proteína C reactiva, dímero D, gasometría arterial).
Para evaluar la severidad de la neumonía por SARS-CoV-2 se utilizó la escala ordinal de la OMS9, siendo la calificación “1” la del COVID-19 con ausencia de síntomas y la calificación “8” para el fallecimiento. El SDRA se definió como la presencia de infiltrados en los cuatro cuadrantes pulmonares que no estén relacionados con otra etiología distinta al COVID-19 sumada a una PaFi <300. Se evaluaron los resultados de gasometría arterial al ingreso, al quinto y al décimo día de tratamiento. El resultado primario fue el tiempo de recuperación, definido como mejoría clínica significativa en la evolución del paciente para considerar el alta. Por lo tanto, se requirió una mejoría subjetiva de la disnea, una reducción del soporte de oxígeno al menos hasta que el mismo estuviera disponible a través de la cánula nasal (si anteriormente estaba con oxigenoterapia con alto flujo, ventilación mecánica no invasiva o ventilación mecánica invasiva) o la suspensión de la misma. Los resultados secundarios fueron el traslado a la unidad de cuidados intensivos, la mortalidad y la sobreinfección.
Estos datos se cargaron en una planilla en Microsoft Excel, se sometió a un control de calidad y posterior análisis con el programa Epi Info 7.2™. Las variables cuantitativas se expresaron en promedio y DE (datos normales), y mediana y RIQ (datos no normales). Las variables cualitativas se expresaron en números absolutos y porcentajes. La comparación del rendimiento de la terapia con dexametasona frente a metilprednisolona se realizó a través de la variable “mortalidad” expresada en números absolutos y porcentajes.
Para este estudio se solicitó autorización a las autoridades del Hospital Nacional de Itauguá, posteriormente se recurrió al Departamento de Bioestadística y a archivos del Hospital Nacional. El protocolo fue sometido a evaluación por el Comité de Ética del Hospital Nacional. Se mantuvo el anonimato de los sujetos del estudio. Se respetaron los Principios de la Bioética. Los autores declaran que no existen conflictos de interés comercial.
RESULTADOS
Se incluyeron a 97 pacientes, de los cuales 52 recibieron dexametasona (grupo 1) y 45 pacientes recibieron metilprednisolona (grupo 2). En la tabla 1 se detallan las características clínico-demográficas y las comorbilidades de cada grupo, las que no mostraron diferencias estadísticamente significativas.
Tabla 1 Características clínico-demográficas de los pacientes con neumonía por SARS-CoV-2 (n 97)
| Dexametasona n 52 (53,6%) | Metilprednisolona n 45 (46,4%) | Valor p | |
|---|---|---|---|
| Sexo | |||
| Femenino | 30 (42,3) | 18 (40) | 0,8 |
| Masculino | 22 (57,7) | 27 (40) | |
| Edad | |||
| Media ± DE | 54,3±16,3 | 57,6±12,9 | 0,3 |
| Grupos etarios | |||
| <65 años | 38 (73,1) | 28 (62,2) | 0,2 |
| ≥65 años | 14 (26,9) | 17 (37,8) | |
| Comorbilidades | |||
| Diabetes mellitus | 11 (21,1) | 16 (35,6) | 0,9 |
| Hipertensión arterial | 25 (48,2) | 22 (48,9) | 0,1 |
| EPOC* | 8 (15,4) | 10 (22,2) | 0,4 |
| Demencia | 5 (9,2) | 1 (2,2) | 0,2 |
| Obesidad | 15 (28,8) | 18 (40) | 0,2 |
| Tabaquismo | 9 (17,3) | 8 (17,8) | 0,9 |
| Insuficiencia cardiaca | 6 (11,5) | 3 (6,7) | 0,5 |
| Falla renal | 6 (11,5) | 5 (11,1) | 0,9 |
*EPOC: enfermedad pulmonar obstructiva crónica
Para evaluar la mediana de la PaFi se realizó un corte <300 a fin de estudiar este valor solo en los pacientes con lesión pulmonar aguda (PaFi entre 201 a 300) o distrés respiratorio (≤200). Del total de 97 pacientes, 82 tuvieron una PaFi <300 al ingreso. No se encontraron diferencias significativas entre ambos grupos con relación al valor de dímero D al ingreso. En la tabla 2 se describe el espectro de enfermedad según la OMS, el dímero D y el porcentaje de antecedente de antibioticoterapia previa al ingreso.
Tabla 2 Características clínicas y laboratoriales de los pacientes con neumonía por SARS-CoV-2 (n 97)
| Variables | Dexametasona n 52 | Metilprednisolona n 45 | Valor p |
|---|---|---|---|
| PaFi | |||
| Mediana (RIQ) | 154 (94-264) | 110 (82-210) | |
| <300 (n,%) | 44 (86,3%) | 38 (84,4%) | 0,8 |
| Dímero D | |||
| Mediana (RIQ) | 757 (562-1362) | 1058 (672-1535) | 0,4 |
| Tratamiento previo | |||
| Antibiótico (n, %) | 24 (48,0) | 16 (37,2) | 0,3 |
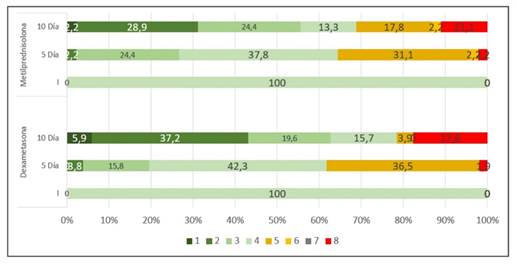
Todos los pacientes del estudio ingresaron con valoración 4 (escala de la OMS). Al quinto día de internación, la mayoría de los pacientes de ambos grupos tenían una clasificación de “4”. Al décimo día 62,7% de los que utilizaron dexametasona fue dado de alta, en comparación con 55,5% de los que recibieron metilprednisolona. En el gráfico 1 se observa la evolución del espectro de la infección SARS-CoV-2 con la escala de la OMS según tratamiento con ambos corticoides.
Trece pacientes (12,6%) ingresaron al servicio de cuidados intensivos, de los cuales 6 (46,2%) recibieron dexametasona y 7 (53,8%) metilprednisolona (p 0,5). Las complicaciones por sobreinfección se presentaron en 29 casos (30%), el foco más frecuente fue el pulmonar. El porcentaje de sobreinfecciones en el grupo que recibió dexametasona fue 15,5% mientras que en el grupo que recibió metilprednisolona fue 14,5% (p 0,7).
La mediana de días de internación general fue 9 días, en los pacientes que utilizaron dexametasona fue ligeramente inferior que en el grupo que utilizó metilprednisolona (8 vs. 10 días) (p 0,09).
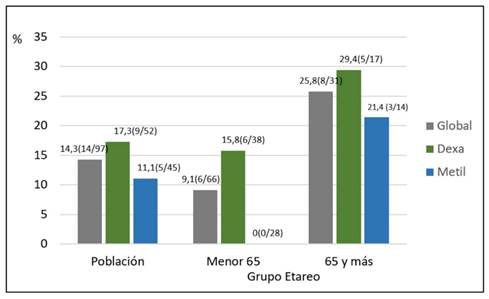
La mortalidad general sin tener en cuenta el tipo de tratamiento fue 14,3%, entre los que recibieron dexametasona fue 17,5% y 11,1% entre los que recibieron metilprednisolona (p 0,4). Luego se estratificó por edades a los pacientes en <65 y ≥65 años. En el grupo de <65 años hubo 66 pacientes, de los cuales 38 recibieron dexametasona y 28 metilprednisolona. Se encontró que la mortalidad entre los que recibieron dexametasona fue 15,8% con un total de 6 fallecidos; mientras que, entre los que recibieron metilprednisolona no hubo fallecidos (p 0,03). En el grupo de ≥65 años hubo 31 pacientes, de los cuales 17 utilizaron dexametasona y 14 metilprednisolona. La mortalidad en el primer grupo fue 29,4% lo que representa un total de 5 fallecidos. En el grupo que recibió metilprednisolona hubo 3 fallecimientos (21,4%) (p 0,7). En el gráfico 2 se señalan los porcentajes de mortalidad según tratamiento y grupo etareo.
DISCUSIÓN
En la actualidad ningún tratamiento presenta eficacia comprobada contra el SARS-CoV-2. El antiviral remdesivir fue aprobado por la Administración de Alimentos y Medicamentos (FDA) de Estados Unidos para su uso contra el SARS-CoV-2, no obstante, debido a su efecto clínico limitado, ha sido muy cuestionado10. La perspectiva actual se ha enfocado a las complicaciones producidas por el virus: distrés respiratorio, síndrome de liberación de citocinas, inflamación sistémica y tisular grave y posterior muerte11. Debido a esto, se han empleado corticoides ya que éstos presentan una potente acción antiinflamatoria. Como referencia histórica, en la epidemia por SARS que ocurrió en el 2003 en China, las manifestaciones clínicas fueron similares a la enfermedad por SARS-CoV-212. Para esta patología se habían comparado diversos tratamientos con antibióticos, antivirales y corticoides. De todas estas alternativas, sólo los pacientes tratados con metilprednisolona en dosis de 160 a 1.000 mg/día durante 5 a 14 días no necesitaron ventilación mecánica y no hubo registro de mortalidad.
En nuestro reporte no se encontraron diferencias significativas en las características clínico-demográficas o analíticas en ambos grupos, ante lo que resulta eficaz la comparación entre ambas muestras. En cuanto a la evaluación por la escala de severidad de la OMS, todos los pacientes ingresaron con valoración “4” en ambos grupos y posteriormente esta valoración fue cambiando, al quinto día de la internación los pacientes que utilizaron dexametasona estaban menos graves (valoración 4) que los que recibieron metilprednisolona (valoración 5). Al décimo día del tratamiento un poco menos de la mitad de los pacientes que recibieron dexametasona había sido dado de alta, porcentaje ligeramente menor en el grupo de metilprednisolona. No se encontraron trabajos previos para poder comparar nuestros resultados. El mayor porcentaje de fallecidos se vio luego de 10 días del tratamiento, con esto podemos inferir que los pacientes con cuadros graves que no mejoran en los primeros 5 días del tratamiento tienen más riesgo de sufrir un desenlace fatal.
La mayoría de los estudios realizados hasta la fecha compararon el resultado clínico entre los pacientes que utilizaron corticoides vs. placebo. Sin embargo, son escasos los estudios que comparan el desenlace clínico entre poblaciones que utilizan corticoides diferentes. Uno de ellos es el desarrollado por Pinzón y col. en donde evaluó las diferencias en el desenlace clínico y laboratorial de pacientes tratados con dosis altas de dexametasona o metilprednisolona. Los pacientes del grupo dexametasona evolucionaron a SDRA grave en una proporción mayor (26,1% frente a 17,1% en el grupo metilprednisolona). Al completar 4 días de tratamiento con corticosteroide parenteral, los marcadores paraclínicos de gravedad disminuyeron significativamente en el grupo que recibió metilprednisolona, con proteína C reactiva de 2,85 (IC 95% 2,3-3,8) frente a 7,2 (5,4-9,8) (p<0,0001), dímero D 691 (IC 95% 612-847) frente a 1083 (IC 95% 740-1565) (p 0,04). Estos hallazgos contrastan con los nuestros, debido a que no encontramos diferencias significativas en la evolución en ambos grupos.
En un estudio observacional comparativo de pacientes con neumonía por SARS-CoV-2 se comparó a aquellos que recibieron 125 a 250 mg/día de metilprednisolona durante 3 días con los que no la recibieron. Los HR ajustados para muerte o muerte e intubación e ingreso a unidad de cuidados intensivos para el primer grupo fueron de 0,35 (IC 95% 0,11 a 1,06; p 0,064) y 0,33 (IC 95% 0,13 a 0,84; p 0,020), respectivamente11. En nuestro estudio, no hubo diferencias significativas en el número de pacientes que ingresaron a cuidados intensivos. No obstante, habría que medir la cantidad de pacientes que requirieron ingreso a terapia intensiva, ya que este estudio fue desarrollado en pleno pico de la pandemia y muchos de nuestros pacientes no pudieron acceder a cuidados intensivos a pesar de su estado delicado de salud.
A pesar de haber empleado dosis altas de corticoides no hubo un aumento significativo de sobreinfecciones. Se registró 15% de sobreinfección con el uso de la dexametasona frente a 14% con metilprednisolona. Otra complicación observada fue la hiperglicemia que estuvo presente en ambos grupos.
En un hospital de alta complejidad de Medellín se llevó a cabo un estudio que evidenció que el grupo de pacientes que recibió metilprednisolona tuvo una menor mortalidad y un tiempo menor de recuperación en comparación con los pacientes que recibieron dexametasona. La mortalidad fue 9,5% para el grupo de metilprednisolona frente a 17,1% del grupo de dexametasona. El tiempo de recuperación fue más corto en los pacientes tratados con metilprednisolona, tres días (3-4) frente a dexametasona 6 días (5-8) (p <0,0001)8.
En nuestro estudio se evaluó las diferencias en la mortalidad de los pacientes que recibieron dexametasona o metilprednisolona. En el grupo de <65 años se demostró que en los tratados con dexametasona la mortalidad fue mucho más alta (15,8%) que entre los que recibieron metilprednisolona, ya que en este último grupo no se registraron fallecimientos, aunque sin diferencia estadísticamente significativa. Esta diferencia en la mortalidad puede estar sujeta a un efecto dosis-dependiente del corticoide. En el grupo de pacientes con ≥65 años, la mortalidad para los tratados con dexametasona o metilprednisolona no tuvo diferencias significativas. Tampoco se encontraron variaciones significativas en la mortalidad global. Creemos que no haber encontrado diferencias en la mortalidad en los pacientes >65 años puede deberse a la edad avanzada propiamente dicha o que los mismos presentan un porcentaje mayor de comorbilidades. No obstante, debido a que nuestra muestra es pequeña, se deberían realizar estudios con mayor número de sujetos a fin de caracterizar más a fondo las particularidades de este grupo etario.
La principal fortaleza de nuestro estudio es que todos los pacientes hospitalizados durante el tiempo establecido recibieron el mismo tratamiento, sin selección, por lo que se pudieron realizar comparaciones en ambos grupos de manera efectiva. Las principales limitaciones fueron el diseño no aleatorizado y sin cegamiento, el tamaño pequeño de la muestra y que se desarrolló en un solo centro. Deberían realizarse estudios multicéntricos con mayor cantidad de participantes a fin de evaluar posibles variables dispersoras como el número de comorbilidades en los grupos de mayor mortalidad. Estas limitaciones impiden la generalización de nuestros hallazgos.
CONCLUSIONES
No se encontraron diferencias significativas de las características clínico-demográficas en los pacientes de ambos grupos. La totalidad de los pacientes tenían una clasificación de “4” de la escala de la OMS al momento del ingreso en ambos grupos, no se encontraron hallazgos significativos en la progresión de dicha escala.
No se encontraron diferencias significativas en cuanto al requerimiento de ingreso a cuidados intensivos. El 14% de los pacientes que recibieron dexametasona presentaron sobreinfecciones, la mayoría de ellas a punto de partida pulmonar. Mientras que en el grupo de pacientes que utilizaron metilprednisolona este porcentaje fue ligeramente mayor (15%). No obstante, este hallazgo no arrojó diferencias significativas.
La mediana de días de internación general fue de 9 días, en los pacientes que utilizaron dexametasona fue ligeramente inferior que en el grupo que utilizó metilprednisolona (8 vs. 10 días), diferencia no significativa.
La mortalidad fue más elevada en los pacientes < 65 años que utilizaron dexametasona en comparación con los que utilizaron metilprednisolona. En cuanto a la mortalidad general, no hubo diferencias significativas.