INTRODUCCIÓN
Una de las mejores alternativas, desde un punto de vista ambiental, para la eliminación de los lodos de depuradora EDARs urbanas es el reciclado a través de su uso en agricultura en el enmendado de suelos como abono, bien de forma directa (después de un tratamiento simple) o tras ser sometidos a un proceso adecuado de compostaje. Sin embargo, estos lodos, pueden representar una de las principales rutas por la que numerosos contaminantes orgánicos potencialmente peligrosos reingresan al medio ambiente (Benítez-Villalba et al., 2017; Doughton& Ternes, 1999; Fent et al., 2006; Jemba, 2006).
En este sentido, existen numerosos aspectos que requieren especial atención para que puedan ser aplicados con suficiente garantía. En primer lugar, es necesario conocer con exactitud la magnitud de su contaminación química, por la posible presencia de numerosas sustancias químicas de origen antropogénicas, así como la variabilidad espacial y temporal de su distribución. En segundo lugar, se desconocen las condiciones de operación óptimas para su eliminación total durante los procesos de compostaje y su evolución en los suelos agrícolas una vez enmendados con dicho material. En tercer lugar, se desconocen los diferentes mecanismos a través de los cuales pueden ser eliminados definitivamente, y las rutas posibles de reingreso y/o permanencia en el medio ambiente, y mucho menos los factores que pueden promover y/o estimular los procesos biológicos a nivel del suelo, que son los que al fin y al cabo pueden asegurar la eliminación definitiva de estas sustancias (Benítez-Villalba et al., 2017; Petrovic et al., 2005; Díaz-Cruz & Barceló, 2006; Temes & Joss, 2006).
En los últimos años se ha generado una nueva preocupación en relación a un grupo más extenso de compuestos orgánicos, los llamados “contaminantes emergentes”, de los que se conoce muy poco sobre su persistencia, evolución en aguas y en suelos agrícolas, su comportamiento durante los procesos de depurado de aguas residuales, mecanismos de degradación, transferencia a la cadena trófica, y efectos adversos sobre los ecosistemas y la salud humana.
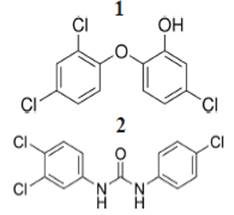
Figuras 1-2: Estructura Química de los compuestos estudiados. 1) Triclosán (TCS). 2) Triclocarbán (TCB).
Esta evidencia justifica el temor de algunos países, con respecto al reciclado de los lodos de desecho en agricultura, especialmente a nivel de la industria alimentaria. El control de estas sustancias se ha ido desarrollando a medida que avanza el conocimiento científico sobre ellas (Kinney et al., 2006).
Esta problemática muestra la necesidad de investigación científica, a nivel químico, biológico, microbiológico, toxicológico y ecológico, con objeto de completar la información ya existente en relación a los contaminantes orgánicos regulados, incluyendo los “contaminantes emergentes” (European Commission, 1996).
Los compuestos seleccionados para este estudio son el triclosán (Figura 1) y triclocarbán (Figura 2); el triclosán, 5-cloro-2-(2,4-dicloro-fenoxi) fenol, se utiliza desde hace más de 40 años como agente antimicrobiano en desodorantes, jabones, cremas y, especialmente, en productos de higiene dental. Es un antiséptico utilizado en productos hospitalarios y productos de consumo (colutorios, desodorantes, dentífricos). Su mecanismo de acción no es muy conocido, pero parece que difunde a través de la membrana citoplasma bacteriana e interfiere su metabolismo lipídico (Singer et al.2002; Jones 2000). En las dosis de uso normales actúa como bactericida, y en dosis menores tiene efecto bacteriostático (Veldhoen et al., 2006; Veldhoen et al., 2007).
El triclocarbán, N-(4-clorofenil)-N’-(3,4-diclorofenil) urea, se usa desde 1957 como agente antimicrobiano en numerosos productos de cuidado personal, especialmente jabones, a niveles de hasta el 1.5 % (p/p) (Council of the European communities, 1976; Scientific committee on consumer products, 2005; TCB consortium, 2002; European Commission, 2011). Existen dudas sobre los posibles efectos negativos del TCS y TCB sobre la salud humana y animal. El estudio llevado a cabo por Veldhoen en 2006 concluye que una dosis reducida de TCS puede actuar como disruptores endocrinos en animales (Veldhoen et al., 2006). El hallazgo hace sospechar que podría tener el mismo efecto en los seres humanos (Veldhoen et al., 2007)
En este trabajo se ha llevado a cabo un estudio cinético y degradación de antimicrobianos en suelo agrícola P1 y suelo agrícola contaminado con compost procedente de lodos de depuradora P2
Utilizando la técnica de extracción por ultrasonido (USE) para extraer los analitos objetos de estudio de las matrices involucradas utilizando para su cuantificación la Cromatografía de Líquidos de Ultra Presión (UPLC) acoplada a Espectrometría de Masas en Tándem (MS/MS, QqQ)
MATERIALES Y MÉTODOS
Productos químicos y reactivos Productos químicos y reactivos
Se utilizaron reactivos de grado analítico. Los patrones de Triclosán y Triclocarbán y el patrón interno Ácido Meclofenámico (AMC) fueron suministrados por la casa comercial Sigma Aldrich (St. Louis, MO). Las soluciones de TCS y TCB (200 mg. mL-1) se prepararon en metanol mensualmente y se almacenaban a -20 °C. Las soluciones estándar, mezclas de estos compuestos junto con el patrón interno se prepararon en metanol o en la fase móvil inmediatamente antes de su uso. Estos estándares se almacenaban a 4°C y se preparaban semanalmente. Todas las soluciones se almacenaron en botellas de vidrio oscuro. El agua y metanol que se utilizaron para la preparación de la fase móvil fueron de grado LC-MS suministradas por Fluka (St. Louis, MO, EE.UU.). El amoníaco (> 25%), acetonitrilo, y acetato de etilo se adquirieron de Merck (Darmstadt, Alemania). El agua (18,2 MΩ cm) se purificó por un sistema Millipore Milli-Q (Bedford, MA, ESTADOS UNIDOS).
Instrumentación y software
Para la recolección de las muestras de compost se emplearon palas convencionales y para las muestras de suelos un muestreador de calado (superficiales) y una barrena helicoidal para mayores profundidades.
El trabajo experimental se desarrolló utilizando una sonda de ultrasonidos Digital Sonifier S450D (BRANSON). Un cromatógrafo Waters Acquity UPLCTM acoplado a espectrómetro de masas triple cuadrupolo Waters H-Class-Xevo TQSTM. La separación de los compuestos se obtuvo con una columna ACQUITY UPLC BEHTM C (1,7µm; 2,1 mm × 50 mm) (Waters). Una fuente de ionización por electroespray Z-sprayTM ESI para la detección de los analitos. El software utilizado para la detección e integración de los picos fue el MassLynx V.4.1 SCN.803 programa de gestión y tratamiento de los datos obtenidos por el cromatógrafo Waters Acquity UPLCTM H-Class - Xevo TQSTM. Un Vortex (Yellow line, Wilmington, NC, USA), una centrifuga Hettich Zentrifugen, universal 32 (Tuttlingen, Alemania). Para el estudio cinético se utilizó un software Statgraphics Plus versión 5.0 (Manugistics, Rockville, MD, EE.UU., 2000). Paquetes Microsoft® Office: Word®, Excel® y PowerPoint® 2007.
Desarrollo Experimental Estudio de campo (TCS y TCB)
Este estudio se realizó con el objetivo de evaluar el comportamiento de los analitos (TCS y TCB) en un determinado ambiente natural, donde los contaminantes pueden ser aportados por diferentes vías. En todos los experimentos llevados a cabo se hizo uso de la irrigación forzada.
Descripción de las Parcelas Experimentales3
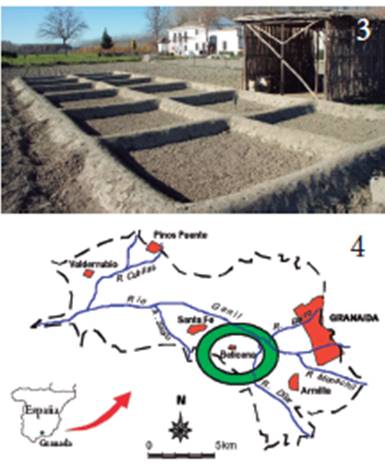
Figuras 3-4: Lugar de estudio. 3) Parcela experimental: Huerta de Santa María. 4) Zona de la Vega de Granada.
El estudio de campo se llevó a cabo en una par- cela experimental (Figura 3) que está situada en la Huerta de Santa María en la Vega de Granada- España en el municipio de Belicena a 5 km de la capital y de coordenadas 37° 11’09.50’’ N; 3° 41’39.85’’ O (Figura 4). En el suelo agrícola no se ha utilizado ningún tipo de pesticida, herbicida o insecticida en los últimos 10 años con el objetivo de no alterar la microbiota del suelo (Kinney et al., 2006).
Las muestras de compost fabricado a partir de lodos de depuradora que fueron utilizados para este ensayo, fueron recolectadas en la empresa compostadora “Biomasa del Guadalquivir” situada en Santa Fe (Granada). Se prepararon una serie de subparcelas de 4 m2 (2 x 2 m) para cada ensayo separadas por tasquibas de 30 centímetros de espesor. Se procedió a la limpieza de la vegetación existente para evitar posibles interferencias en los mecanismos de adsorción- desorción, la degradación de los compuestos en estudio, o la interferencia sobre alguna variable general como el índice de evaporación del agua. Se fijaron dos condiciones diferentes, Parcela 1 (P1) contaminantes puros aplicados directamente al suelo. Parcela 2 (P2) enmendada con compost y contaminada con TCS y TCB.
La contaminación tanto de la parcela compostada como de la no compostada se realizó adicionando 1 g.L-1 de cada compuesto en un volumen de 120 litros de agua de pozo. Una vez dopada, durante todo el periodo de experimentación se llevaron a cabo sucesivamente dos operaciones, una de muestreo y otra de riego. La toma de muestra se realizó a siete profundidades (superficie, 10, 20,30, 40, 50 y 60 centímetros) a lo largo del tiempo (0, 15 y 30 días). Durante la primera semana la toma de muestra fue diaria, ya que estudios previos realizados habían demostrado que durante este espacio de tiempo se producía la caída exponencial de la concentración, aportando información de gran importancia sobre el comportamiento del compuesto.
Tratamiento de la muestra
Cada una de las muestras tomadas se sometió a las siguientes etapas para asegurar su correcto análisis en el laboratorio. Adición de formaldehido 1 % (m/v), para evitar el crecimiento microbiano en las muestras. Secado y tratamiento de las mues- tras, en bandejas de plástico y al sol a temperatura ambiente. Una vez secas se molturaron con un mortero de hierro y se tamizaron con ayuda de una malla de 2 mm. Posteriormente se introdujeron en una bolsa de plástico y se llevaron al laboratorio donde permanecieron a una temperatura de 4oC hasta su análisis. Una vez en el laboratorio, las muestras de suelo fueron analizadas. Para este ensayo se realizaron en total 12 tomas de muestra a diferentes tiempos.
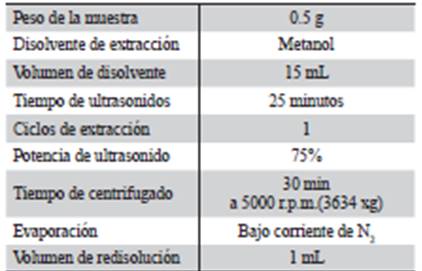
La técnica de extracción seleccionada para la extracción de los analitos fue la técnica de ultrasonidos pos su mayor simplicidad y menor coste. Las variables utilizadas para la extracción de las muestras dopadas con los compuestos (100 μg g-1) se pueden observar en la Tabla 1, las condiciones utilizadas.
Análisis mediante UPLC-MS/MS
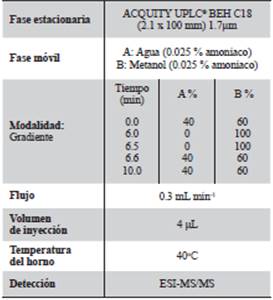
La determinación y cuantificación de la cantidad de los compuestos degradados se realizó mediante la técnica de UPLC-MS/MS, empleando las condiciones descritas en la Tabla 2. Se muestran los parámetros optimizados para la separación cromatográficas y la detección mediante espectrometría de masas. Una vez optimizadas estas variables se seleccionaron las dos transiciones en el espectrómetro (cuantificación e identificación) óptimas para la determinación de cada molécula. En la Tabla 3 se muestran las transiciones seleccionadas.
RESULTADOS
Determinación de la concentración del analito Parcela 1
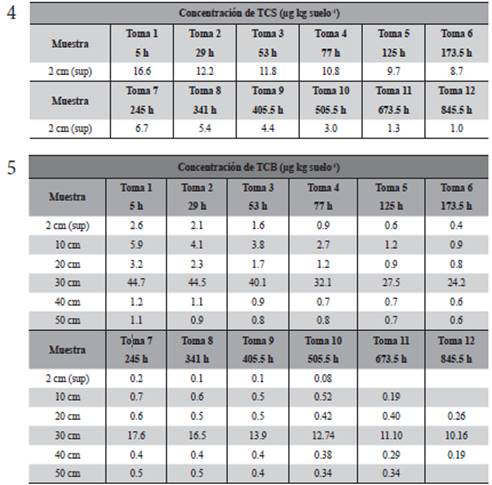
En las Tablas 4 y 5 se muestran las concentraciones de cada analito en las muestras de suelo contaminadas.
Cinéticas de Desaparición de los Compuestos en el Suelo (Parcela 1)
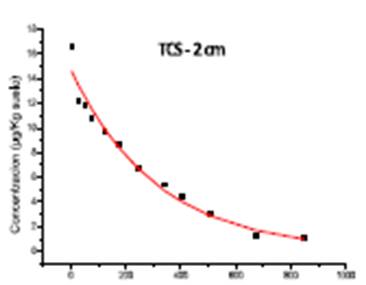
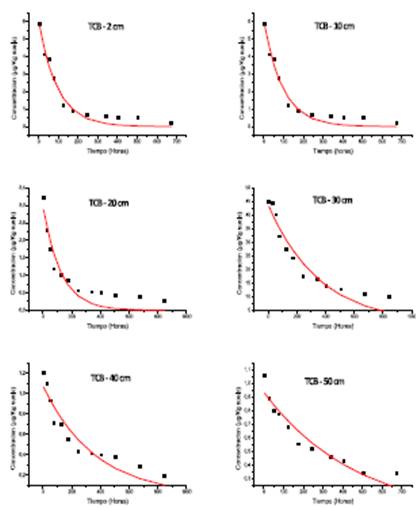
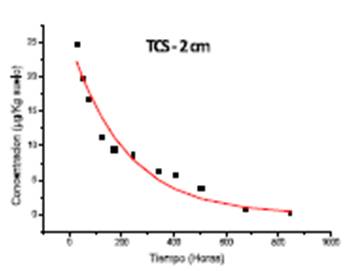
La variación de las concentraciones de todos los contaminantes estudiados en el suelo agrícola contaminado, a las distintas profundidades, como consecuencia de los procesos adsorción-desorción, transporte y degradación, permite deducir que el proceso de desaparición de los compuestos, en cada uno de los puntos de toma de muestra, sigue una cinética de primer orden. Este modelo se rige por la siguiente ecuación C = C 0 e-kt , donde, C representa la concentración de analito (µg kg suelo-1) a un tiempo determinado t (min), C0 concentración inicial del analito (µg kg suelo-1) y k es una constante cinética (h-1) (Figuras 5 y 6).
Tabla 3: Parámetros del espectrómetro de masas para el TCS y TCB. CV: Voltaje del cono; CE: Energía de colisión.
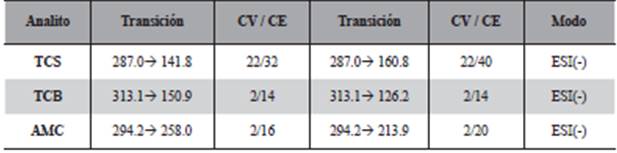
Tabla 4: Concentraciones de TCS y TCB en el tratamiento en la parcela 1. 4) Concentraciones de TCS. 5) Concentraciones de TCB.
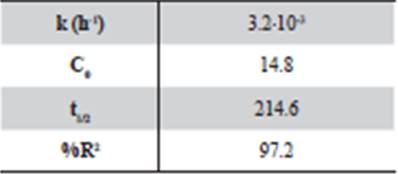
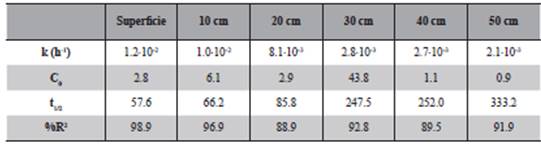
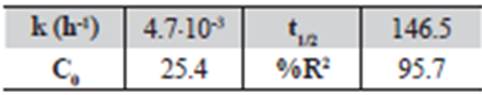
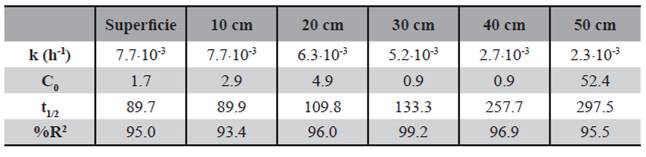
Los datos mostrados en las figuras, se ajustan, en todos los casos, a la ecuación exponencial de primer orden anteriormente citada (C= C0 .e-kt). A partir de los datos, se obtuvieron los correspondientes valores de la constante de desaparición del compuesto (k), el tiempo de vida media en cadazona del suelo (t) y coeficiente de determinación (R2) (Tablas 6 y 7).
Al igual que en otros casos, el TCS se adsorbe y desaparece en la superficie no lixiviando a mayores profundidades. La degradación del TCS en el suelo fue relativamente rápida con los tiempos de vida media 214.6 h.
Por último, el TCB se detecta en los primeros 50 cm, no lixiviando a la mayor profundidad de 60 cm. La desaparición del compuesto fue rápida con tiempos de vida media comprendidos entre las 57.6 h en la capa superficial a las 333.2 h a los 50 cm de profundidad.
Además, y como era de esperar, debido a los fenómenos de degradación y lixiviación principal- mente, al establecer la relación entre las constantes obtenidas, se constata que la velocidad de desaparición del compuesto es mayor cuanto más cerca k sup > k 10 cm > k 20 cm > k 30 cm > k 40 cm. . La explicación de la superficie se encuentra el analito, de forma radica en que parte del compuesto se degrada y otra parte migra por arrastre con el agua hacia puntos inferiores tras cada uno de los regados.
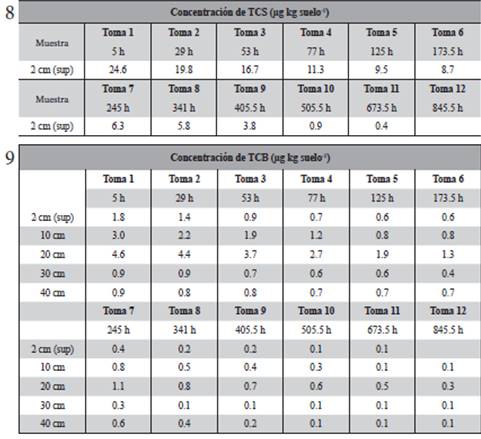
Tablas 8-9. Concentración de TCS y TCB en el tratamiento en la parcela 2. 8) Concentración de TCS. 9) Concentración de TCB.
Determinación de la concentración del analito Parcela 2
Finalizado el estudio en la parcela 1 (suelo con los analitos puros), se repitió el proceso de la misma forma, pero en este caso empleando una parcela que previamente había sido enmendada con compost procedente de lodo de depuradora (parcela 2) tal y como se describió con anterioridad. En las Tablas 8 y 9 se muestran los datos de concentración obtenidos en los análisis de las diferentes muestras tomadas a las distintas profundidades.
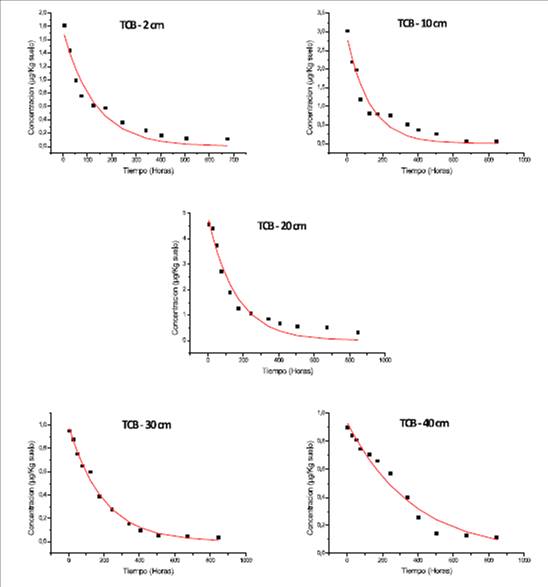
Los resultados mostrados en las tablas demuestran que al igual que en el caso del estudio realizado en la primera parcela, el TCS es retenido en la superficie (2 cm), degradándose completamente en este punto. Por último, el TCB, aparece hasta profundidades de hasta 40 cm.
Cinéticas de Degradación de los Compuestos en Suelos Enmendados con Compost (Parcela 2)
Al igual que en el caso del primer experimento llevado a cabo en la parcela 1, la observación de la variación de las concentraciones con el tiempo, a las distintas profundidades, permite vaticinar una cinética de primer orden para todos casos estudiados (C= C0 e-kt) (Figuras 7 y 8).
A continuación, partiendo de los datos de concentración obtenidos para cada profundidad, se obtuvieron los parámetros correspondientes de la ecuación exponencial de primer orden C= C0. e-kt, es decir, los valores de la constante de desaparición del compuesto (k), el tiempo de vida medio (t1/2) y el coeficiente de determinación (R2). Las Tablas 10 y 11 muestran los valores obtenidos.
En todos los casos, el comportamiento es similar al observado en la parcela 1, aunque con ciertas diferencias que desarrollaremos a continuación.
Comparación del Comportamiento de los Contaminantes en Suelo y en Suelo Enmendado con Compost
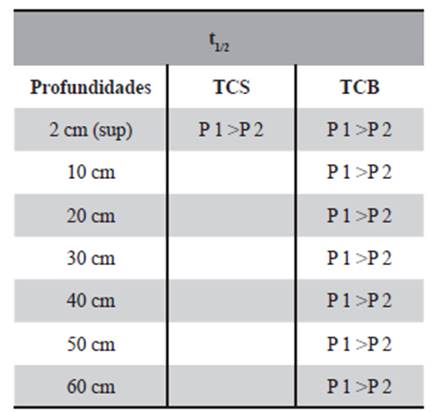
Durante este estudio comparativo de la cinética de degradación de estos compuestos en suelos y suelos enmendados con compost se demuestra que, los analitos estudiados en las diferentes condiciones, tienen un comportamiento similar, ajustándose en todos los casos a una cinética de primer orden. En la Tabla 12 se comparan los tiempos de vida media de cada uno de los compuestos estudiados a las distintas profundidades, en ambos estudios.
Los resultados de este trabajo muestran como el tiempo de vida media de los dos analitos es superior para las condiciones de la parcela P1 (suelo con los contaminantes puros aplicados directamente al suelo). En el caso del TCS, se puede observar que sólo se absorbe y degrada en la superficie en ambas condiciones, mostrando que el tiempo de vida medio es mayor en las condiciones de la P1. Finalmente, en el caso del TCB, se aprecia que el compuesto aparece hasta la máxima profundidad estudiada (60 cm), pudiendo incluso lixiviar a mayores profundidades. En todos los casos el tiempo de vida media fue mayor bajo las condiciones de la parcela P1.
DISCUSIÓN
La fertilidad de los suelos agrícolas está íntimamente ligada a su microbiota particular y a las relaciones que existen entre los grupos microbianos involucra- dos en los ciclos de los nutrientes, los cuales son esenciales para el funcionamiento y la evolución normales del suelo (Paul et al., 2006).
En este sentido resulta muy aprovechable el uso de compost en los suelos agrícolas ya que produce un incremento de los microrganismos que son beneficiosos para los cultivos (Bigeriego Martín de Saavedra et al., 2000). Es sabido que un suelo fértil es aquel que contiene una reserva adecuada de elementos nutritivos disponibles para las plantas o bien una población microbiana capaz de aportar nutrientes que permitan un buen desarrollo de los vegetales (Beltrán et al., 2006).
El compost aporta al suelo materias orgánicas y en general nutrientes que proporciona mejoras al suelo agrícola dado que favorece simultáneamente el desarrollo de la comunidad bacteriana del suelo (Álvarez et al., 1997). La microbiota del suelo es la responsable de la descomposición de la materia orgánica, la producción de humus, fijación del nitrógeno atmosférico, solubilizarían de nutrientes esenciales como el fósforo, control biológico de plagas y enfermedades, descomposición de xenobióticos y otros (Moreira & Siqueira, 2002).
Por todo lo dicho anteriormente podemos decir que en este trabajo de investigación podemos observar como un enriquecimiento de materia orgánica a la parcela P2 con compost acelera el tiempo de vida media produciendo un crecimiento de la microbiota del suelo que hace que en la presencia de estos compuestos químicos lo utilicen como fuente de carbono y energía. Por lo tanto, dicha microbiota podrían ser utilizados como biorremediacion en algunos ambientes contaminados.
CONCLUSIÓN
Como conclusión general, se observa que, en la mayoría de los compuestos, los tiempos de vida media son mayores en las condiciones experimentales de la parcela P1. Desde el punto de vista medio ambiental el enmendado de los suelos agrícolas con compost es muy beneficioso porque aporta materia orgánica, hecho que favorece el crecimiento de microorganismos que provoca el fenómeno de la biodegradación de estos contaminantes emergentes que en dosis reducida pueden actuar como disruptores endocrinos en animales e incluso seres humanos.












 uBio
uBio