INTRODUCCION
El tratamiento de las arritmias cardíacas y los trastornos de la conducción con la implantación de un marcapasos o desfibrilador implantable puede presentar diferentes complicaciones. La endocarditis infecciosa (EI) relacionada con dispositivos cardíacos se destaca por ser una de las más desafiantes en cuanto a su diagnóstico y manejo. Ocurre con baja frecuencia, pero es una de las complicaciones más graves asociada con una significativa morbilidad, mortalidad y carga económica para los sistemas de salud.
Los eventos embólicos son una complicación frecuente y potencialmente mortal de la endocarditis infecciosa (EI), pero siempre más evaluada en EI izquierdas. En cuanto a la EI derecha y eventos embólicos se conocen pocos datos y refieren una alta adaptabilidad de la vasculatura pulmonar con una menor mortalidad y morbilidad de la embolia pulmonar (EP). Presentamos el caso de una paciente con diagnóstico actual de EI asociada a marcapasos, que luego de la extracción del dispositivo por vía percutánea presentó síntomas de embolia pulmonar confirmada mediante estudios por imágenes.
REPORTE DE CASO
Paciente de 68 años, sexo femenino, con historia de implante de marcapaso definitivo bicameral 2 años antes de la consulta. Recambio de generador y cables un año más tarde por decúbito de bolsillo. Consulta al servicio de clínica médica por cuadro febril de 10 días de evolución sin foco evidente. Al ingresar no presentaba datos de relevancia en el examen físico. Los resultados del laboratorio demostraron leucocitosis con formas inmaduras en la fórmula y eritrosedimentación aumentada. En base al cuadro y para continuar con su evaluación, se internó en el Departamento de Clínica Médica. Los hemocultivos fueron positivos para Staphylococcus aureus meticilino resistente. Ante la sospecha de EI se solicitó un ecocardiograma transesofágico donde se observó catéter auricular y ventricular con múltiples imágenes móviles compatibles con vegetaciones con un diámetro longitudinal de hasta 22 mm (Figura 1).

Figura 1. ETT de ingreso que muestra una vegetación de 22 x 0,9 mm en el catéter de la aurícula derecha
Con el diagnóstico confirmado de EI asociada a DEIP, se instauró la terapéutica recomendada (Antibiótico endovenoso utilizando vancomicina más rifampicina y retiro completo del dispositivo). La extracción del dispositivo se realizó por vía percutánea utilizando vainas y estiletes. Inmediatamente luego de la extracción refirió disnea y dolor torácico. Ante la sospecha de EP se solicitó un centellograma ventilación-perfusión que la confirmó (Figura 2). Durante el episodio no presentó caída en la saturación de oxígeno ni inestabilidad hemodinámica. En un nuevo ecocardiograma transtorácico no se detectaron signos de compromiso del ventrículo derecho por la EP (Solamente insuficiencia tricúspidea leve) ni hipertensión pulmonar o dilatación de la vena cava inferior. Gasometría arterial, troponina ultrasensible y pro-BNP normales.
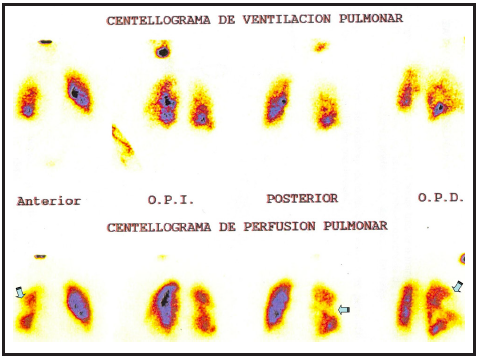
Figura 2. Gammagrafia pulmonar: A) fase ventilatoria que muestra distribución regular del aerosol radiactivo en ambos pulmones. B) fase de perfusión que presenta fundamentalmente zona hipoperfundida en el pulmón derecho en forma cónica
Los hemocultivos tomados durante la continuación del tratamiento con antibióticos y después de la finalización del mismo fueron negativos, y los análisis de laboratorio estuvieron dentro de los rangos normales. El reimplante del dispositivo se realizó luego de dos semanas de tratamiento antimicrobiano. Completó el esquema antibiótico durante 6 semanas y fue dada de alta. Luego de 18 meses de seguimiento evolucionó sin complicaciones cardiológicas ni infectológicas.
DISCUSION
En primer lugar, mencionaremos que las principales complicaciones de la EI asociada a DEIP se dividen en valvulares (locales) y no valvulares (periféricas). Dentro de las primeras encontramos la insuficiencia valvular (tricúspidea y pulmonar), estenosis valvular, absceso de anillo. Dentro de las periféricas describiremos:
a) Pulmonares: embolismo, infiltrados, abscesos y derrame pleural.
b) Embolia e infartos sistémicos (émbolo paradójico a través del foramen oval permeable u otra comunicación entre cavidades derechas-izquierdas).
c) Shock séptico y/o falla multiorgánica.
De todas ellas, las complicaciones más comunes incluyen insuficiencia valvular, formación de abscesos y embolia pulmonar. En una revisión reciente, se informó compromiso pulmonar en el 80% de los casos de EI derechas y varió desde infiltrados, embolia pulmonar hasta abscesos 1-3. Si nos focalizamos en la EP, los datos de las autopsias reportaron casos asintomáticos en el 8% a 10% de los pacientes con DEIP 3. En otros trabajos publicados encontramos datos de incidencia de EP sintomático en el 0-5% 2-5. La embolia se puede dar tanto antes como durante el procedimiento de extracción percutánea del dispositivo.
En cuanto al riesgo de embolia, algunos autores consideran que tanto antes como durante la extracción transvenosa de catéteres con vegetaciones de más de 10 mm el riesgo de embolismo pulmonar es mayor que para vegetaciones menores a 10 mm 1-6. Observamos una tendencia hacia un mayor riesgo de EP post extracción percutánea del dispositivo en pacientes con vegetaciones mayores de 20 mm 3. En vegetaciones sobre tejido endocárdico o valvular que pueden presentarse en pacientes con este tipo de EI, otro factor de riesgo de embolia es la movilidad de la vegetación, como lo demuestran las investigaciones sobre el riesgo de embolia en la endocarditis de válvula nativa 7. Según publicaciones, aunque normalmente está relacionado con bacterias como Staphylococcus aureus, también se ha observado que las infecciones fúngicas causan EP 2,4.
En cuanto al inicio de los signos y síntomas de EP, se pueden presentar tanto antes como luego de la extracción del dispositivo. Los síntomas más frecuentes fueron disnea y dolor pleurítico, y los signos más frecuentes fueron taquipnea y taquicardia 3. En los casos publicados, la confirmación de EP se realizó con angiografía por tomografía computada y en el resto con otras modalidades de imagen, como la gammagrafía pulmonar nuclear con ventilación y perfusión, como fue en nuestro caso 3-4.
Una pregunta que deberíamos hacernos sería: ¿Cómo podemos prevenir la EP? Como sabemos, la EI se caracteriza por la formación de una vegetación en la superficie de la válvula cardíaca, compuesta por bacterias, plaquetas, fibrina y leucocitos.
Los estudios in vitro sugirieron que el aumento de la activación plaquetaria juega un papel central en la fisiopatología de la EI. Estos estudios demostraron que los microorganismos involucrados en la patogenia de la EI pueden interactuar con las plaquetas y los factores de coagulación. Gérmenes como el Staphylococcus aureus y su factor de virulencia, desencadenan mayor adhesión plaquetaria e inducen directamente la agregación plaquetaria y activación de factores de la coagulación. Esto facilita la formación de vegetaciones de mayor tamaño que promueven eventos tromboembólicos. Sobre esos datos fisiopatológicos surgieron investigaciones acerca del uso del ácido acetilsalicílico, antagonista del receptor plaquetario P2Y12 y anticoagulantes. Sin embargo, los datos relacionados a este tema fueron controvertidos porque algunos estudios no mostraron que previniera los eventos tromboembólicos 8-10. Otro factor asociado a una reducción del riesgo de embolia pulmonar es el tiempo trascurrido desde el inicio del tratamiento antibiótico efectivo. Se ha demostrado que una vez iniciada la terapia con antibióticos, la tasa de embolia disminuye drásticamente. En distintas publicaciones se evidenció que la tasa de embolización disminuye drásticamente luego de dos semanas de tratamiento antibiótico efectivo. El control de la infección juega un papel principal en la prevención de la embolia 11-12.
En cuanto al tratamiento, lo recomendado por la bibliografía es el uso antibiótico endovenosos durante 4 a 6 semanas y retiro del sistema en forma completa. La extracción del dispositivo puede realizarse por vía percutánea, o en caso de no ser factible, esternotomía y circulación extracorpórea para realizar atriotomía. El manejo de las vegetaciones grandes sigue siendo controvertido, y la declaración de consenso de expertos de la Heart Rhythm Society de 2017 incluyó grandes desórdenes de cables (> 2,5 cm) entre las razones para justificar las morbilidades asociadas con la cirugía a corazón abierto 13. Sin embargo, no hay normas específicas para el tamaño de una vegetación antes de tomar una decisión invasiva (percutáneo o técnicas quirúrgicas abiertas).
Sin embargo, la morbilidad y la mortalidad no fueron influenciadas por esta complicación y puede explicarse por el grado de severidad del compromiso de la circulación pulmonar y la naturaleza del material embolizante. Las vegetaciones (fibrina, microorganismos, plaquetas y células inflamatorias) son material friable y menor tamaño en contraste con las firmes y grandes de los trombos venosos en el tromboembolismo pulmonar. Otros factores que podrían influenciar son los antecedentes cardiológicos y respiratorios del paciente, el inicio precoz de antibióticos y la extracción temprana del dispositivo en centro con experiencia.
CONCLUSION
La EP es una complicación poco frecuente en la EI asociada a DEIP. Se observó más frecuentemente en vegetaciones de más de 10 mm con mayor movilidad y asociadas a infecciones por Staphylococcus aureus. En cuanto al inicio de los signos y síntomas de EP, se puede presentar tanto antes como luego de la extracción del dispositivo. Los síntomas más frecuentes fueron disnea y dolor pleurítico, y los signos más frecuentes fueron taquipnea y taquicardia. La confirmación de EP se realizó con angiografía por tomografía computada o gammagrafía pulmonar nuclear con ventilación y perfusión. A pesar de la EP en este grupo de pacientes, la morbimortalidad intrahospitalaria y durante el seguimiento posterior no se vio influenciada, probablemente debido a las características del material embolizante. Otros factores que podrían influenciar son los antecedentes cardiológicos y respiratorios del paciente, el inicio precoz de antibióticos y la extracción temprana del dispositivo en centro con experiencia. Realizamos la descripción de un caso poco frecuente de EP por una EI asociada a DEIP que presentó respuesta favorable a un tratamiento combinado.
Contribución de los autores:
Gabriel Pérez Baztarrica: revisión y corrección del manuscrito, discusión. Gabriela Tripicchio: revisión y corrección del manuscrito, discusión del caso. Paul Solorzano Berrospi: revisión del manuscrito e imágenes. Luis Gabriel Castro Orozco: recopilación de datos clínicos y seguimiento de la paciente. Nadia Juliana Chiriboga: recopilación de datos clínicos y seguimiento de la paciente. Robert Chamorro Ortega: recopilación de datos clínicos e imágenes. Edin Maldonado Cubas: revisión y corrección del manuscrito. Diego Gallardo Astudillo: recopilación de datos clínicos. Jessica Rocha Zamora: búsqueda bibliográfica. Jaime Pérez Pérez: búsqueda bibliográfica.
Los autores confirman que el manuscrito es una investigación original que no ha sido publicada y no está bajo consideración en ningún otro lugar. Confirmar que todos los autores participaron en la preparación del manuscrito y redacción, revisión crítica del artículo o revisión del contenido y aprobación final de la versión a ser enviada.
Conflicto de intereses: no tenemos conflictos para divulgar cualquier relación comercial, financiera, personal o de otro tipo con otras personas u organizaciones que puedan influir de manera inapropiada en nuestro trabajo.
Financiación: el trabajo ha sido realizado con recursos propios.















