INTRODUCCIÓN
La gonorrea es una infección causada por la bacteria Neisseria gonorrhoeae, diplococo Gram negativo, la cual es transmitida a través del contacto con exudados de las membranas mucosas de un individuo infectado, casi siempre como resultado de actividad sexual sin protección1.
Actualmente la infección gonocócica es la segunda ITS de etiología bacteriana más prevalente, tras la causada por Chlamydia trachomatis. N. gonorrhoeae representa un problema de salud pública importante, tanto por su magnitud como por las complicaciones y secuelas a que da lugar. Debido a la ausencia de vacunas efectivas, un diagnóstico apropiado, así como un tratamiento antimicrobiano efectivo, son dos herramientas principales para evitar la diseminación de la infección2.
La Organización Mundial de la Salud (OMS) estima que, en el 2012, se produjeron 78 millones de nuevos casos de gonorrea en adolescentes y adultos de 15 a 49 años en todo el mundo, con una tasa de incidencia mundial de 19 por 1000 mujeres y de 24 por 1000 hombres. La prevalencia estimada de 27 millones de casos de gonorrea en el 2012 se tradujo en una prevalencia mundial de gonorrea de un 0,8% en las mujeres y de un 0,6% en los hombres de 15 a 49 años3.
Desde un punto de vista histórico, los compuestos antimicrobianos utilizados en el tratamiento de la gonorrea, han visto comprometida su eficacia debido a la capacidad de N. gonorrhoeae de desarrollar mecanismos de resistencia. La resistencia a penicilina y tetraciclina comienza en los años 1970 y se extendió por el mundo en los 80. Progresivamente, las penicilinas, sulfamidas y tetraciclinas dejaron de ser la primera elección en las infecciones por N. gonorrhoeae, precisando el empleo de nuevos antimicrobianos4.
N. gonorrhoeae puede portar plásmidos que producen una enzima penicilinasa, también llamada Beta-lactamasa (B-lactamasa) que inactiva las penicilinas. La determinación de B-lactamasa provee una información rápida en cuanto a la resistencia a penicilina y ampicilina de aislamientos de N. gonorrhoeae. Todos los aislamientos que producen B-lactamasa son clínicamente resistentes a penicilina, ampicilina y algunas cefalosporinas4.
Las primeras cepas de N. gonorrhoeae con CMI a ciprofloxacino ≥ 1 ug/ml se aislaron fundamentalmente en el Extremo Oriente: Hong Kong, Filipinas y Japón, que luego se extendió a Estados Unidos, asociándose con la aparición de fracasos terapéuticos. En las últimas recomendaciones del CDC de Atlanta, se describe que la resistencia a quinolonas está ampliamente extendida en el mundo y ya no se recomienda para la gonorrea, por consiguiente, solo las cefalosporinas se mantienen como alternativa5.
Entre 1987-2008 en Estados Unidos, la proporción de cepas con sensibilidad disminuida a ceftriaxona detectada fue de 4 casos y con sensibilidad disminuida a cefixima 48 casos, por lo que se mantuvieron como tratamiento recomendado5.
En el año 2007, el Grupo de Apoyo de la Sociedad de Enfermedades Infecciosas de Estados Unidos, había manifestado que “La Neisseria gonorrhoeae se ha sumado a la lista de superbacterias para las cuales las opciones terapéuticas se volvieron peligrosamente “escasas”5.
En cuanto a los mecanismos de resistencia, N. gonorrhoeae puede desarrollar uno o varios mecanismos a la vez a diferentes antimicrobianos que son utilizados para el tratamiento. Según el fenotipo de resistencia que presenten las cepas, OPS/OMS propone una nomenclatura para su mejor clasificación y determinar el fenotipo circulante más frecuente, que se basa en los resultados del perfil de susceptibilidad obtenidos6.
Actualmente, el método de diagnóstico más recomendado para la detección de N. gonorrhoeae es el cultivo bacteriano, acompañado de un frotis del fluido y tinción de Gram. También se recomienda que a las cepas aisladas se les realice las pruebas de susceptibilidad antimicrobiana. La identificación de especie se alcanza con las pruebas bioquímicas; otros métodos de diagnóstico confirmatorios se basan en ensayos moleculares a través de pruebas de amplificación de ácidos nucleicos a partir de muestras biológicas6.
Alerta de emergencia de la resistencia a cefalosporinas: En Estados Unidos en el período 2000-2010, hubo un aumento en el porcentaje de cepas con cifras elevadas de concentración inhibitoria mínima a cefalosporinas (>0.25 ug/ml. para cefixima y ≥ 0.125 ug/ml para ceftriaxona). En este contexto, la recomendación fue que los laboratorios de referencia se mantuvieran alerta a los niveles de resistencia a cefalosporinas y los clínicos a los potenciales fracasos de tratamiento. Para esto, es vital la mantención del cultivo de N. gonorrhoeae para fines de vigilancia7.
En el 2010, en Japón se identificó desde frotis faríngeo de una trabajadora sexual, la primera cepa de N. gonorrhoeae resistente a ceftriaxona, lo que amenaza el control de la enfermedad. La CIM de ceftriaxona para este aislamiento fue de 2 ug/ml. Esta cepa se denominó N. gonorrhoeae H041, siendo caracterizada como el clon ST7363, lo que corresponde a la secuencia tipo predominante entre los clones resistentes a cefixima. Los estudios siguientes sugirieron que la cepa era sensible solo a azitromicina y espectinomicina. En este caso la erradicación de la infección en faringe fue exitosa, aunque se considera un hábitat temporal por no ser un sitio ideal para el desarrollo del agente8.
En este escenario la bacteria ha demostrado una capacidad sorprendente para resistir las defensas del ser humano, capacidad para adquirir en tiempos relativamente breves resistencia a antibióticos, hasta llegar a la situación actual en que ya se utilizan cefalosporinas de tercera generación para su tratamiento efectivo (8.
En julio de 2011, la Organización Panamericana de la Salud / Organización Mundial de la Salud (OPS/OMS), emitieron una Alerta Epidemiológica sobre N. gonorrhoeae multirresistente, con el siguiente comunicado: “Ante la identificación en ámbitos científicos de una cepa de gonorrea resistente a todos los microbianos disponibles para tratamiento de ITS, la Organización Panamericana de la Salud recomienda informar a los trabajadores de salud, instituciones y organizaciones no gubernamentales que trabajan en la prevención y control de las ITS sobre el riesgo de la resistencia de esta cepa y en particular fortalecer la vigilancia en cada país ante la aparición de cepas con un perfil inusual. También se recomienda promover el empleo de métodos para prevenir las ITS”9.
En febrero de 2018, ante el número creciente de infecciones por N. gonorrhoeae con resistencia a las cefalosporinas de espectro extendido, la OPS/OMS recomendó a los Estados Miembros fortalecer la vigilancia y la capacidad de diagnóstico de los laboratorios para apoyar la detección de casos, proporcionar el tratamiento indicado e identificar las poblaciones en alto riesgo. Además, recordó que la prevención y el manejo adecuado de casos constituyen la medida esencial para mitigar la resistencia a los antimicrobianos10.
Aunque se ha documentado aumento de la resistencia gonocócica a los medicamentos antimicrobianos, tan solo un 36% de los países de la Región de las Américas realizan una vigilancia sistemática de esta resistencia para respaldar las decisiones de tratamiento. Los primeros casos de infección por N. gonorrhoeae resistente a la ceftriaxona se notificaron en 2007. Desde entonces y hasta octubre de 2017, Argentina, Brasil, Canadá y los Estados Unidos identificaron infecciones por este microorganismo11.
Actualmente el CDC recomienda una terapia mixta con cefalosporina (ceftriaxona 250 mg) más azitromicina o doxiciclina11.
Situación de la resistencia en Paraguay: desde el año 2005, el LCSP coordina la vigilancia de la resistencia de aislamientos de N. gonorrhoeae, con el objetivo de identificar y registrar los perfiles de susceptibilidad a los antimicrobianos. Así, a partir de 2012 según los resultados de la Red de Vigilancia Laboratorial de la RAM, se describe un progresivo incremento de la resistencia de N. gonorrhoeae a penicilina, ciprofloxacina y tetraciclina; antimicrobianos usados generalmente para el tratamiento de la gonorrea12.
El LCSP, a través la Sección Antimicrobianos del Dpto. de Bacteriología y Micología, forma parte de la Red Internacional GASP-LAC (Gonococcal Antimicrobial Surveillance Programme in Latin America and the Caribbean), cuyo objetivo es reforzar las redes de Salud Pública que investigan la emergencia de resistencia antimicrobiana en aislamientos de N. gonorrhoeae en América Latina y el Caribe, a través de la estandarización y control de calidad externo, liderado por el Laboratorio Regional de Referencia de ITS para América del Sur INEI-MALBRAN, Argentina6,13.
Hasta la fecha, en nuestro país, aún no se ha notificado alguna cepa resistente a cefalosporinas de espectro extendido14, por lo que es imperiosa la vigilancia de esta bacteria para la detección precoz ante la tendencia de la aparición de alguna cepa multirresistente y la inclusión de antígenos de clones representativos de la región para el potencial desarrollo de una vacuna gonocócica15.
Teniendo en cuenta todo el contexto expuesto, se realizó este estudio, cuyo objetivo principal fue determinar la susceptibilidad a los antimicrobianos utilizados en el tratamiento de la gonorrea y detectar los distintos fenotipos de resistencia de cepas de N. gonorrhoeae enviadas al LCSP por los Laboratorios colaboradores de la Red de Vigilancia Laboratorial de la RAM por el lapso de un año.
MATERIALES Y MÉTODOS
Se estudiaron 157 cepas remitidas al LCSP como N. gonorrhoeae, que fueron aisladas de muestras clínicas de pacientes pediátricos y adultos, en el marco de la vigilancia de la RAM, desde enero a diciembre de 2021. En un primer paso se determinó la viabilidad de las cepas y la confirmación de la identificación, para lo cual, las cepas remitidas se repicaron en medio agar chocolate enriquecido con suplementos vitamínicos (agar Choco Poli) y en agar Thayer Martin, y posteriormente se incubaron en estufa de CO2 a 36°C por 24 a 48 hs. Posteriormente, la identificación de las cepas se realizó por los “métodos presuntivos” y “métodos confirmatorios”, siguiendo las guías del Laboratorio Regional de Referencia de ITS14.
Para la identificación presuntiva se utilizaron las siguientes pruebas: coloración de Gram del cultivo, test de oxidasa y la prueba del superoxol con agua oxigenada al 30% de concentración, que se basa en la intensidad de producción de burbujas que es característica de esta especie.
La identificación confirmatoria se realizó basada en sus patrones de producción de ácido a partir de carbohidratos (glucosa, maltosa, lactosa, fructosa y sacarosa), en el medio Agar Cistina Tripteína (CTA) con una concentración final del azúcar al 1%.
La prueba de susceptibilidad antimicrobiana se realizó por el método de difusión de discos (Kirby Bauer) en el medio agar GC enriquecido con 1% de suplemento vitamínico para los siguientes antimicrobianos: penicilina 10 U, ciprofloxacina 5 ug, tetraciclina 30 ug, ceftriaxona 30 ug, cefixima 5 ug y azitromicina 15 ug. Las placas se incubaron en CO2 por 20 a 24 hs para su posterior lectura e interpretación según las guías del Clinical Laboratory Standards Institute (CLSI) 202116.
La detección de B-lactamasa se realizó por el método iodométrico en tiras de papel. Este método se basa en que el ácido penicilinoico, producido por la acción de la betalactamasa sobre el anillo B-lactámico de la penicilina, reduce el yodo a yoduro, por tanto, decolora la mezcla de almidón-yodo empleada para visualizar la reacción. La detección es realizada siguiendo los siguientes pasos: Se coloca una tira en una placa de Petri vacía, se humedece con Lugol (la tira toma un color azul negro) y se aplica una ansada del aislamiento sobre la tira. Si la tira se decolora dentro del minuto, la prueba es positiva.
Para el control de calidad de medios y discos de antibióticos se utilizó la cepa patrón de N. gonorrhoeae ATCC 49226 y para el control de las tiras de Beta-lactamasa la cepa N. gonorrhoeae ATCC 31426.
Para caracterizar los fenotipos de resistencia hallados en este estudio, se utilizó la nomenclatura propuesta por OPS/OMS (6, denominándose según la definición como:
PPNG: NG productora de penicilinasa. Cepa con resistencia plasmídica a penicilina: β-lactamasa positiva, CIM ≥ 2 μg/ml, usualmente halo de inhibición ≤ 19 mm.
CMPR: Cepa con resistencia cromosómica a penicilina: β-lactamasa negativa, CIM ≥ 2 μg/ml, halo de inhibición ≤ 26 mm
TRNG: NG con resistencia plasmídica a tetraciclina, CIM ≥ 16 μg/ml, halo de inhibición ≤ 19 mm.
CMTR: Cepa con resistencia cromosómica a tetraciclina, CIM ≥ 2 μg/ml, halo de inhibición ≤ 30 y >19 mm.
PP-TRNG: NG con resistencia plasmídica a penicilina y tetraciclina.
CMRNG: Cepas con resistencia cromosómica a penicilina y tetraciclina.
QRNG: NG con resistencia cromosómica a quinolonas. En el caso de resistencia a ciprofloxacina puede nombrarse también como CIPR
AZNS: NG no susceptible a azitromicina (CIM ≥ 2 μg/ml).
C3GNS: NG no susceptible a cefalosporinas de tercera generación (CIM ≥ 0,5 μg/ml para ceftriaxona o cefixima), halo de inhibición ≤ 34 mm para ceftriaxona o ≤ 30 mm para cefixima.
SENSIBLE: Incluye cepas con sensibilidad intermedia y sensible según tablas de CLSI.
Es importante considerar que pueden existir distintas combinaciones de estos fenotipos. Ej.: PPQRNG/CMTR.
Las cepas se congelaron a -80 ◦C en caldo cerebro corazón (BHI) con adición de glicerol al 20% para la realización posterior de estudios moleculares.
Todos los datos obtenidos en este estudio fueron registrados en una planilla del Software Excel 2010 y posteriormente analizados utilizando estadística descriptiva.
RESULTADOS
De las 157 cepas remitidas, fueron viables 139, que fueron incluidas en este estudio para confirmar la identificación y posteriormente realizar la prueba de susceptibilidad. De estas cepas viables, 11 correspondieron a otras especies de Neisseria u otras bacterias. Se confirmaron en total 128 cepas como N. gonorrhoeae.
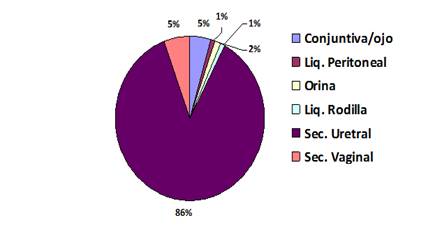
De las 128 cepas identificadas como N. gonorrhoeae, 87% (111/128) correspondieron a secreción uretral y el resto a otros sitios de infección como se muestra en la Figura 1.
Según los datos demográficos obtenidos, el 93% (119/128) de los aislamientos procedieron de pacientes del sexo masculino con un promedio de edad de 29 años, y el 7% (9/128) del sexo femenino, también con un promedio de edad de 29 años. Por la importancia del hallazgo, podemos mencionar que se confirmaron cepas de N. gonorrhoeae aisladas de secreción genital en 2 menores de edad, y en secreción ocular en 3 menores de edad. En la Figura 2 se detalla la frecuencia de hallazgo según sexo y grupos etarios.
En cuanto a la susceptibilidad antimicrobiana de las cepas de N. gonorrhoeae confirmadas, la resistencia a penicilina fue 48% (61/128) y sensibilidad intermedia 52% (67/128), no obteniéndose cepas sensibles a este antibiótico. Con ciprofloxacina la resistencia fue 70% y con tetraciclina 19%. Además, el 100% de las cepas fueron sensibles a azitromicina, ceftriaxona y cefixima en el periodo estudiado, como se puede observar en la Tabla 1.
Tabla 1. Porcentaje de resistencia a los antimicrobianos en N. gonorrhoeae. Año 2021. N=128.
| Interpretación* | |||
|---|---|---|---|
| %R | %I | %S | |
| Penicilina G | 48 | 52 | 0 |
| Ciprofloxacina | 70 | 13 | 16 |
| Tetraciclina | 19 | 17 | 64 |
| Ceftriaxona | 0 | 0 | 100 |
| Cefixima | 0 | 0 | 100 |
| Azitromicina | 0 | 0 | 100 |
*CLSI (Clinical and Laboratory Standards Institute); R: resistente; I: sensibilidad intermedia; S: sensible.
Se realizó el estudio de producción de B-lactamasa a todas las cepas, y se detectó un 45% (58/128) de positividad. De todas las cepas resistentes a penicilina, 5% (3/61) dieron B-lactamasa negativa.
Los fenotipos de resistencia se caracterizaron basándose en el perfil de sensibilidad que presentaron las cepas de N. gonorrhoeae siguiendo la nomenclatura de OPS/OMS, encontrándose que la mayor frecuencia correspondió al tipo QRNG (resistencia a ciprofloxacina) con 40% (51/128), seguido de los fenotipos PPNG-QRNG (resistencia a penicilina y ciprofloxacina) con 15% (19/128), como se muestra en la Tabla 2.
Tabla 2. Nomenclatura de fenotipos de resistencias (OPS/OMS).
| Fenotipos de resistencias | Descripción | % de hallazgo |
| QRNG | R a quinolonas | 40% |
| PPNG-QRNG | R plasmídica a penicilina y R a quinolonas | 15% |
| PPNG | R plasmídica a penicilina | 13% |
| SENSIBLE | Sin resistencia | 11% |
| PP-TRNG-QRNG | R plasmídica a penicilina y tetraciclina con R a quinolonas | 5% |
| PPNG-CMTR-QRNG | R plasmídica a penicilina con R cromosómica a tetraciclina y quinolonas. | 5% |
| CMPR-QRNG | R cromosómica a penicilina y quinolonas. | 2% |
| PP-TRNG | R plasmídica a penicilina y tetraciclina | 2% |
| PPNG-CMTR | R plasmídica a penicilina con R cromosómica a tetraciclina | 2% |
| CMTR-QRNG | R cromosómica a tetraciclina y quinolonas. | 2% |
| CMPR | R cromosómica a penicilina | 2% |
| CMRNG-QRNG | R cromosómica a penicilina y tetraciclina | 1% |
R: resistencia.
DISCUSIÓN
La frecuencia del sitio de infección, como era de esperarse, fue de secreción uretral en un 87%. En cuanto a la frecuencia de acuerdo al sexo y edad, se pudo constatar la mayor proporción en adultos del sexo masculino en un 93% con un promedio de edad de 29 años. Por la importancia del hallazgo, podemos mencionar que se confirmó N. gonorrhoeae en 3 menores de edad del sexo femenino aislada de muestras genitales y en 2 menores de edad del sexo masculino aislada de secreciones oculares.
Estos datos son comparables con las tasas de incidencia y prevalencia proporcionadas por OPS/OMS3.
El análisis de los resultados de la susceptibilidad antimicrobiana revela el alto porcentaje de resistencia de N. gonorrhoeae circulantes en el país; así, para penicilina se obtuvo 48% de resistencia y 52% de sensibilidad intermedia, y para ciprofloxacina un 70% de resistencia; quedando evidenciada la escasa actividad de estas drogas contra este patógeno.
Según los últimos datos de la Red Latinoamericana de Vigilancia de la Resistencia a los Antimicrobianos (ReLAVRA), la resistencia ha venido aumentando de forma sostenida, de tal manera que se han reportado en la región datos de hasta 71% de resistencia a penicilina, 32% de resistencia a tetraciclina; y para ciprofloxacina, las cepas aisladas han aumentado la resistencia en un promedio del 62%13.
Con la prueba de la Beta-lactamasa se pudo comprobar en este estudio, que la mayor frecuencia de resistencia a penicilina fue por el mecanismo plasmídico. Este dato coincide con otros hallazgos en diferentes países que han notificado este mecanismo de resistencia desde 19804.
Por otro lado, desde 2007 en América Latina y el Caribe se están reportando aislamientos con sensibilidad reducida a las cefalosporinas de espectro extendido, y desde entonces el número de casos ha ido en aumento6,13. En Paraguay, hasta la fecha, no hemos detectado cepas “no sensibles” a estas cefalosporinas.
Se confirmó que el fenotipo más frecuente fue QRNG (40%), que proporciona resistencia a quinolonas, seguido del fenotipo PPNG-QRNG (15%) con resistencia a penicilina y ciprofloxacina, situación similar reportada por otros países a través de los datos GASP-LAC6.
Ante la evolución de la resistencia a los antimicrobianos en este patógeno, es imperiosa la necesidad de seguir trabajando en la vigilancia, capacitando a los profesionales bacteriólogos, mejorando las técnicas de aislamiento e implementando la metodología de referencia para el estudio de susceptibilidad.